Cum funcționează CRISPR
Imaginează-ți că ai putea deschide „codul sursă” al vieții și să corectezi o greșeală de tipar care provoacă o boală gravă. Sună a science-fiction? Nu mai este. Tehnologia CRISPR face exact asta — și deja salvează vieți. În decembrie 2023, primul tratament bazat pe CRISPR a fost aprobat oficial de FDA, iar în 2026 sunt în desfășurare peste 150 de studii clinice care vizează totul, de la cancer la boli genetice rare. Dar cum funcționează de fapt această tehnologie revoluționară? Și ce înseamnă ea pentru viitorul medicinei?
Ce este CRISPR, pe scurt?
CRISPR este o prescurtare de la „Clustered Regularly Interspaced Short Palindromic Repeats” — un nume lung pentru un concept surprinzător de simplu. La bază, CRISPR este un sistem natural de apărare pe care bacteriile îl folosesc de milioane de ani pentru a se proteja de viruși. Când un virus atacă o bacterie, aceasta „memorează” o bucată din ADN-ul virusului și o stochează în propriul genom, ca un fel de dosar cu amprentele infractorilor. Dacă același virus atacă din nou, bacteria îl recunoaște instant și îl distruge.
Cercetătorii au realizat că acest mecanism poate fi transformat într-un instrument de editare genetică extrem de precis. În loc să caute viruși, sistemul poate fi programat să caute orice secvență de ADN din orice organism — inclusiv din celulele umane.
Cum funcționează CRISPR-Cas9: mecanismul în 3 pași
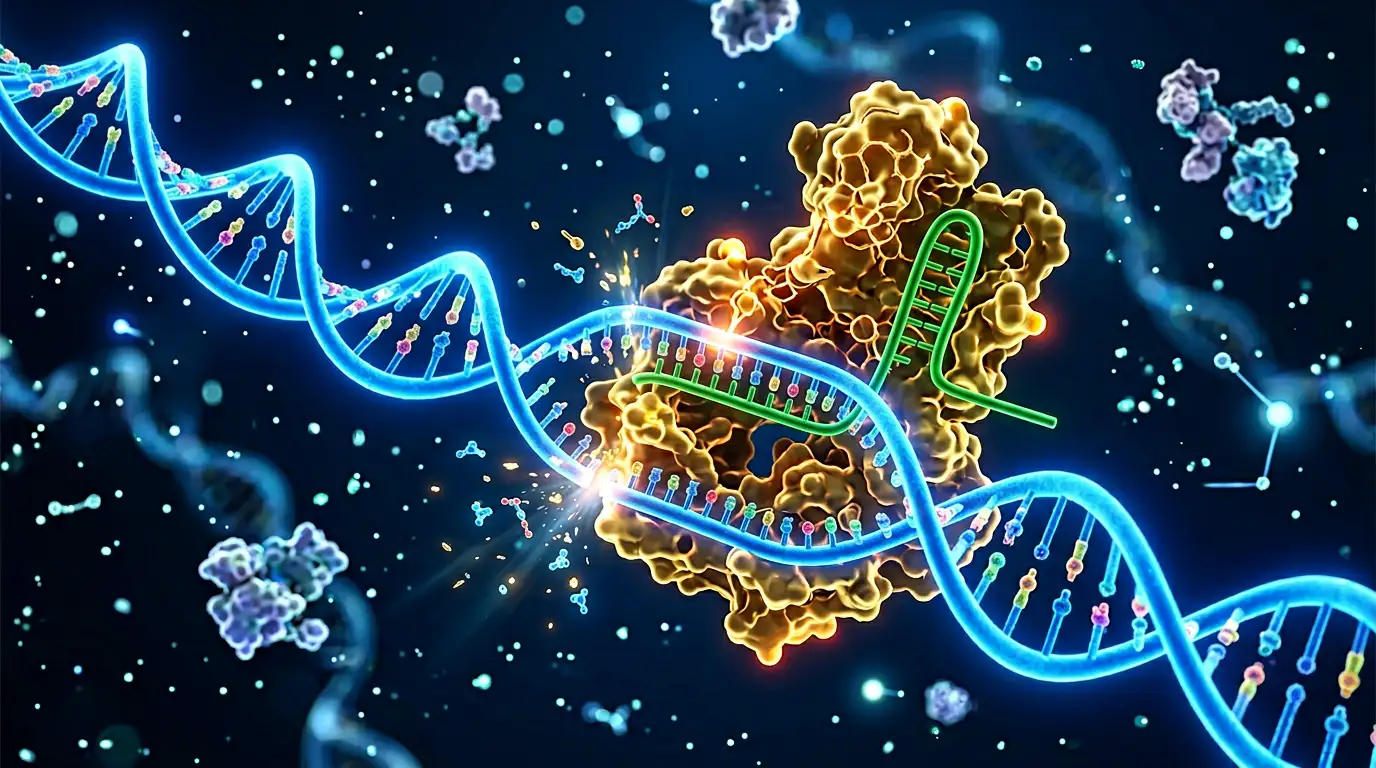
Întregul proces se bazează pe două componente principale: un ARN ghid (care știe exact unde să meargă) și o enzimă numită Cas9 (care taie ADN-ul). Gândește-te la ARN-ul ghid ca la un GPS molecular, iar la Cas9 ca la o foarfecă microscopică de precizie chirurgicală.
Pasul 1 — Căutarea țintei. Cercetătorii proiectează un ARN ghid care se potrivește perfect cu secvența de ADN pe care vor să o modifice. Acest ARN ghid „scanează” genomul celulei până găsește locul exact — ca atunci când folosești Ctrl+F într-un document uriaș cu 3 miliarde de caractere.
Pasul 2 — Tăierea. Odată ce ARN-ul ghid s-a atașat de secvența țintă, enzima Cas9 taie ambele catene ale ADN-ului în acel punct precis. Practic, se creează o ruptură controlată, exact acolo unde vrem noi.
Pasul 3 — Repararea. După tăietură, celula își activează mecanismele naturale de reparare. Aici lucrurile devin interesante, pentru că cercetătorii pot exploata acest proces în două moduri. Primul: celula repară ruptura „pe repede-înainte”, introducând mici erori care dezactivează gena respectivă — util atunci când vrem să oprim o genă defectă. Al doilea: cercetătorii furnizează celulei o „șablon” de ADN corect, pe care aceasta îl copiază în locul secvenței originale — practic, o corecție chirurgicală a codului genetic.
Pe scurt, CRISPR-Cas9 este un sistem de „găsește și înlocuiește” pentru ADN — programabil, precis și revoluționar de simplu comparativ cu metodele anterioare de editare genetică.
Cine a descoperit CRISPR? Povestea din spatele Premiului Nobel
Povestea modernă a CRISPR începe în 2011, când două cercetătoare s-au întâlnit la o conferință științifică: Jennifer Doudna de la Universitatea din California, Berkeley, și Emmanuelle Charpentier de la Institutul Max Planck din Germania.
În iunie 2012, cele două au publicat studiul care a schimbat lumea biologiei. Au demonstrat pentru prima dată că sistemul CRISPR-Cas9 poate fi programat să taie ADN-ul bacterian în locuri precise — deschizând calea pentru editarea genetică la scară largă.
În 2020, Doudna și Charpentier au primit Premiul Nobel pentru Chimie pentru descoperirea „foarfecelor genetice” CRISPR/Cas9. A fost prima dată în istorie când două femei au împărțit acest premiu, un moment simbolic pentru comunitatea științifică. Comitetul Nobel a descris descoperirea ca având „un impact revoluționar asupra științelor vieții, contribuind la dezvoltarea de noi terapii împotriva cancerului și având potențialul de a vindeca boli genetice.”
Aplicații medicale reale: CRISPR în 2025-2026
CRISPR nu mai este doar un subiect de laborator. Iată cum schimbă deja medicina.
Casgevy — prima terapie CRISPR aprobată
În decembrie 2023, FDA a aprobat Casgevy (exagamglogene autotemcel), prima terapie din istorie bazată pe CRISPR-Cas9. Tratamentul vizează anemia falciformă, o boală genetică în care globulele roșii se deformează și blochează vasele de sânge, provocând dureri extreme și leziuni ale organelor.
Cum funcționează? Medicii prelevează celule stem din sângele pacientului, le editează genetic în laborator folosind CRISPR pentru a reactiva producția de hemoglobină fetală (o formă de hemoglobină care previne deformarea celulelor), apoi le reinjectează pacientului. Rezultatele sunt remarcabile: 94% dintre pacienții tratați nu au mai avut crize de durere timp de cel puțin un an. Casgevy a fost aprobat ulterior și pentru beta-talasemia, o altă boală genetică a sângelui, și este disponibil în SUA, Regatul Unit, UE, Canada și alte țări.
CRISPR împotriva cancerului
În 2025-2026, peste 150 de studii clinice active folosesc CRISPR în lupta împotriva cancerului. Cea mai promițătoare abordare implică editarea celulelor imunitare ale pacientului (celule T sau celule CAR-T) pentru a le transforma în „soldați” mai eficienți împotriva tumorilor.
Rezultatele timpurii sunt încurajatoare. În mai 2025, un studiu a arătat că celulele imunitare editate cu CRISPR au produs răspunsuri semnificative la pacienți cu cancer de colon metastatic care nu mai răspundeau la tratamentele standard. Cel mai impresionant caz: un pacient a avut un răspuns complet — tumorile au dispărut și nu au mai revenit timp de peste doi ani.
Cercetările vizează și cancerele de rinichi, col uterin, pancreas, esofag și plămâni, transformând CRISPR într-o armă din ce în ce mai versatilă în arsenalul oncologic.
Boli genetice rare
CRISPR deschide ușa către tratarea unor boli considerate până recent incurabile. Printre cele aflate în studii clinice avansate se numără boala de stocare a glicogenului de tip I, imunodeficiența combinată severă legată de X (X-SCID) și cardiomiopatia amiloidă cu transtiretină, unde un tratament experimental (NTLA-2001) a demonstrat o reducere de peste 90% a proteinei patogene.
Controversa care a zguduit lumea științifică
Nu poți vorbi despre CRISPR fără să menționezi cazul care a provocat cea mai mare controversă din istoria recentă a geneticii.
În noiembrie 2018, cercetătorul chinez He Jiankui a anunțat că a creat primii bebeluși editați genetic din lume — două fetițe gemene cărora le-a modificat gena CCR5 folosind CRISPR, cu scopul declarat de a le face rezistente la HIV.
Reacția comunității științifice a fost instantanee și categorică: condamnare totală. Motivele erau multiple și grave. Nu exista o justificare medicală reală, deoarece CCR5 putea fi gestionat prin metode convenționale. Protocolul de studiu era prost conceput, iar standardele etice de protecție a subiecților de cercetare nu fuseseră respectate. Mai mult, He Jiankui falsificase certificatul de aprobare etică al spitalului.
Cercetători de renume mondial au calificat experimentul drept „prematur”, „monstruos” și „profund iresponsabil.” Problema fundamentală nu era doar ce făcuse He Jiankui, ci ce ușă deschisese: modificarea germinală — adică editarea ADN-ului care se transmite generațiilor viitoare — ridică întrebări complet diferite față de terapiile somatice precum Casgevy, unde modificările afectează doar pacientul tratat.
He Jiankui a fost condamnat la trei ani de închisoare pentru „practici medicale ilegale.” Cazul a accelerat eforturile internaționale de reglementare a editării genetice germinale și rămâne un memento puternic: puterea CRISPR necesită o responsabilitate pe măsură.
Viitorul CRISPR: ce urmează?
Tehnologia evoluează rapid. Două variante de nouă generație — base editing (editarea de baze) și prime editing (editarea primară) — promit o precizie și mai mare, permițând modificări la nivelul unei singure „litere” din codul genetic, fără să taie ADN-ul. Este ca diferența dintre a șterge un paragraf întreg și a corecta doar o literă greșită.
Cercetătorii lucrează și la terapii in vivo — adică editarea celulelor direct în corpul pacientului, fără a fi necesară prelevarea și reinjectarea lor. Aceasta ar reduce dramatic costurile și ar face tratamentele accesibile unui număr mult mai mare de pacienți.
Pe lista bolilor vizate pentru următorii ani se află Alzheimer, distrofia musculară, hemofilia, HIV, hepatita și diverse forme de cancer. Combinarea CRISPR cu alte imunoterapii ar putea crea tratamente cu adevărat personalizate, adaptate profilului genetic unic al fiecărui pacient.
Surse
- FDA — Aprobarea primelor terapii genice pentru anemia falciformă: fda.gov
- Comitetul Nobel — Premiul Nobel pentru Chimie 2020: nobelprize.org
- Innovative Genomics Institute — Studii clinice CRISPR 2025: innovativegenomics.org
- National Center for Biotechnology Information — Mecanism și aplicații CRISPR: ncbi.nlm.nih.gov
- Science Magazine — Controversa He Jiankui: science.org





